13.02.2006
Basisinfo
Antibiotikaresistenz-Gene als Marker
Erst gebraucht, dann unerwünscht
In gentechnisch veränderten Pflanzen wird die Verwendung von Antibiotikaresistenz-Genen stark eingeschränkt. Doch wozu werden sie gebraucht und warum sind sie umstritten? Einige Fragen und Antworten.
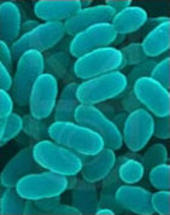
Infektionskrankheiten. Immer mehr Erreger sind resistent geworden gegen Antibiotika. Wenn heute Antibiotika zunehmend ihre Wirksamkeit verlieren, hat das nichts mit gentechnisch veränderte Pflanzen und ihren Markergenen zu tun. (Foto: Streptokokken)
Wozu eigentlich Markergene?
Es gibt verschiedene Verfahren, mit denen neue Gene in das Erbgut von Pflanzen eingeführt werden können. Man kann Teile eines Bodenbakteriums (Agrobacterium tumefaciens) als „Fähre“ benutzen, es ist aber auch möglich, Gene direkt in eine Zelle oder in eine „Zelle ohne Zellwand“ (Protoplasten) einzubringen, etwa mit einer Partikelkanone (Gene Gun). Das Problem: Nur wenige der behandelten Pflanzenzellen werden tatsächlich transformiert. Bei ihnen ist das Fremdgen in das Genom integriert.
Selbst bei einer so gut transformierbaren Pflanze wie Arabidopsis (Ackerschmalwand), der Modellpflanze der Gentechniker, werden nur etwa fünf von 1000 behandelten Zellen tatsächlich gentechnisch verändert - und bei den meisten Pflanzenarten sind es noch weniger.
Um die transformierten Zellen im großen Haufen der nicht transformierten zu finden, sie zu „selektieren“ - dazu braucht man Marker.
Oft werden Markergene außerdem in einer früheren Phase benötigt, wenn die Transformations-Werkzeuge „konstruiert“ und anschließend vermehrt werden. Meist handelt es sich um Bakterien bzw. Plasmide(DNA-Ringe), die als „Verpackung“ (Vektor) für das zu übertragende Fremdgen dienen.
Warum sind Markergene meist Antibiotikaresistenz-Gene?
Markergene sollen transformierte Pflanzenzellen markieren - je einfacher, schneller und zuverlässiger das funktioniert, um so besser. Lange Zeit glaubten die Gentechniker, eine Ideallösung gefunden zu haben: Antibiotika - jene Medikamente, die Ärzte gegen viele Infektionskrankheiten verordnen.
Antibiotika sind natürliche Abwehrstoffe bestimmter Schimmelpilze gegen Bakterien, ihre Konkurrenten. Einige Bakterienarten haben „gelernt“, die gegen sie gerichteten Gifte zu entschärfen: Sie besitzen ein Gen, das ihnen eine Resistenz gegen das Antibiotikum verleiht.
Auf diesem System von „Gift“ und „Gegengift“ beruht die Wirkungsweise der Marker. Ein meist aus Bakterien stammendes Antibiotikaresistenz-Gen wird mit dem Zielgen, das der Pflanze das gewünschte neue Merkmal verleihen soll, gekoppelt. Jede transformierte Zelle, besitzt damit nicht nur das Zielgen, sondern auch das Resistenz-Gen: Im Gegensatz zu normalen Pflanzenzellen kann ihnen das jeweilige Antibiotikum nichts anhaben. Setzt man die Pflanzenzellen auf einen mit dem Antibiotikum getränkten Nährboden, sterben alle Zellen ab - bis auf jene, die das Markergen tragen. Übrig bleiben nur transformierte Zellen.
Warum sind Antibiotikaresistenz-Gene in die Kritik geraten?
Der Erfolg der Antibiotika in der Medizin ist zum Problem geworden. Viele Bakterien, darunter auch Erreger von Infektionskrankheiten, sind bereits resistent und können mit dem jeweiligen Antibiotikum nicht mehr bekämpft werden.
Zu häufig werden Antibiotika in der Human- und Tiermedizin eingesetzt - vor allem aber: Lange Zeit wurden sie dem Tierfutter als Leistungsförderer beigemischt. Inzwischen ist diese Praxis zwar weitgehend verboten - dennoch: Die überall vorhandenen Antibiotika haben jenen Bakterien einen Überlebensvorteil beschert, die ein entsprechendes Resistenz-Gen haben. Den haben sie genutzt. Hinzu kommt, dass die Resistenz-Gene bei den Bakterien oft auf mobilen DNA-Einheiten sitzen, die zwischen verschiedenen Arten ausgetauscht werden können.
Vor diesem Hintergrund wurde befürchtet, Markergene aus transgenen Pflanzen könnten von Bakterien aufgenommen werden. Am Ende könnte es dann zu Krankheitserregern kommen, gegen die derzeit verordnete Antibiotika wirkungslos sind.
Voraussetzung für ein solches Szenario ist ein horizontaler Gentransfer - die Aufnahme von Pflanzen-Genen durch Bakterien. Grundsätzlich ist ein solches Ereignis unter natürlichen Bedingungen möglich, vor allem dort, wo bereits zersetztes oder verrottendes pflanzliches Material auf große Bakterien-Mengen trifft: etwa im Magen-Darm-Trakt von Menschen und Tieren oder in der Mais-Silage.
Sind die Befürchtungen berechtigt?
Bakterien können Pflanzen-Gene aufnehmen - allerdings ist ein solches Ereignis unter natürlichen Bedingen außerordentlich selten. Aus verschiedenen Untersuchungen weiß man inzwischen, dass eine Reihe Bedingungen erfüllt sein müssen, damit Bakterien fremde Gene nicht nur in ihr eigenes Genom einbauen, sondern auch die genetische Information ablesen und in ein Protein umsetzen. Erst dann wird ein Antibiotikaresistenz-Gen wirksam.
Es muss eine Menge zusammenkommen, damit ein horizontaler Gentransfer tatsächlich stattfindet. In der Regel beträgt die Wahrscheinlichkeit, dass ein Bakterium ein Pflanzen-Gen aufnimmt, etwa 1:1 Milliarde bis 1: 100.000 Milliarden.
Dennoch: Völlig auszuschließen ist ein solcher Gentransfer nicht, vor allem wenn bestimmte Bedingungen zutreffen, die seine Wahrscheinlichkeit erhöhen. In einem solchen Fall könnten Krankheitserreger Antibiotikaresistenz-Marker etwa aus verrottenden transgenen Pflanzen aufnehmen.
Allerdings sind solche Resistenzen bei Bakterien ohnehin weit verbreitet. Viele der in Ackerböden anzutreffenden Bakterien besitzen eine Resistenz gegen das Antibiotikum Kanamycin. In drei Vierteln aller aus Schweinen und Rindern isolierten Proben wurden Ampicillin-resistente Bakterien gefunden.
Bei der Bewertung möglicher Gefahren sollte auch berücksichtigt werden, dass die Markergen-Systeme auf verschiedenen Antibiotika-Wirkstoffen basieren. Einige davon spielen in der Tier- und Humanmedizin eine Rolle, viele hingegen werden schon seit längerem nicht mehr verschrieben.
Unerwünschte Antibiotikaresistenz-Marker
Wie immer das tatsächliche Risiko sein mag - Antibiotikaresistenz- Marker sind längst nicht mehr unumstritten. Wenn auch aus unterschiedlichen Gründen empfehlen Behörden und Experten, dass gentechnisch veränderte Pflanzen künftig ohne sie auskommen sollten.
- Bereits 1997 sprach sich die ZKBS - das die deutsche Zulassungsbehörde beratende Expertengremium - dafür aus, bei der Übertragung von Genen sich auf diejenigen zu beschränken, die für das neue, gewünschte Merkmal codieren.
- Die seit 2002 geltende EU-Freisetzungsrichtlinie verlangt eine „schrittweise Einstellung der Verwendung von Antibiotikaresistenz-Markern in GVO, die schädliche Auswirkungen auf die menschliche Gesundheit oder die Umwelt haben können“.
Doch auch in der praktischen Forschung zeigen sich Nachteile der traditionellen Marker.
- Sollen bereits gentechnisch veränderte Pflanzen noch einmal transformiert werden, benötigt man zwei unterschiedliche Markergen-Systeme. Für jede Kulturart stehen jedoch nur wenige zur Verfügung.
- Es kann die Stabilität des gentechnisch vermittelten Merkmals beeinträchtigen, wenn sich mehrere Markergene, die aus verschiedenen Entwicklungsphasen übrig geblieben sind, in einer Pflanze anhäufen.
- Je mehr Gene und Markergene übertragen werden, um so größer die Wahrscheinlichkeit, dass es in den Pflanzen zu unvorhergesehenen Effekten (pleiotrope Effekte) kommen kann.
In der nächsten Generation transgener Pflanzen werden Antibiotikaresistenz-Marker nicht mehr die Regel, sondern die Ausnahme sein. Doch bis genügend neue Verfahren und Strategien für die praktische Pflanzenzüchtung zur Verfügung stehen, ist es noch ein weiter Weg.
Thematische Verknüpfungen
Streitfall Markergene

Im Web
Informationen zu Antibiotikaresistenz- Markergenen:
- EFSA: Europäische Behörde für Lebensmittelsicherheit
- EFSA: Gutachten zu Antibiotikaresistenz-Genen gv-Pflanzen 2004 (Zusammenfassung, deutsch)
- EFSA bewertet Antibiotikaresistenz-Markergene in gentechnisch veränderten Pflanzen (11.06.2009)
- Stellungnahme der Zentralen Kommission für die Biologische Sicherheit (ZKBS) für die Sicherheitsbewertung von Antibiotika-Resistenzgenen im Genom gentechnisch veränderter Pflanzen, Kurzfassung (Dez. 2008)
- Zentrale Kommission für biologische Sicherheit (ZKBS)
- EU-Freisetzungs-Richtlinie (2001/18/EG)
