AIDS-Impfstoff aus Algen
Chlamydomonas reinhardtii auf dem Weg zum Pharma-Star

Chlamydomonas reinhardtii - eine einzellige Grünalge: Test auf erfolgreiche Integration fremder Geninformation für die Herstellung eines potentiellen AIDS-Impfstoffs. (Bildquelle: © Rouhollah Barahimipour)
Arzneistoffe in Algen zu produzieren hat viele Vorteile: Algen sind anspruchslos, wachsen schnell und ressourcenschonend. Außerdem können Algen samt Arzneistoff sogar verzehrt werden, wodurch kostspielige Reinigungsprozesse entfallen. Wissenschaftler haben bisherige Produktionsschwierigkeiten beseitigt und den Weg für die Grünalge Chlamydomonas reinhardtii zum Molecular-Pharming-Star geebnet.
Die einzellige Grünalge Chlamydomonas reinhardtii ist eigentlich ein idealer Organismus zur Produktion pharmazeutischer Produkte. Sie kann sowohl photoautothroph, als auch heterotroph und in einer Mischform wachsen. Alle drei Genome der Alge - im Kern, im Plastid und im Mitochondrium - sind vollständig sequenziert und können stabil und unkompliziert transformiert, also gezielt verändert werden. Chlamydomonas lässt sich zudem leicht in großen Volumen kultivieren. Allerdings gibt es ein paar Haken dabei: Nukleare Transgene, also Fremdgene, die in den Zellkern eingebracht wurden, werden nicht immer in nennenswerten Mengen in die gewünschten Proteine übersetzt. Außerdem werden manche Transgene im Laufe der Zeit durch epigenetische Prozesse wieder stillgelegt. Es scheint, als ob sich die Algen vor dem Kapern ihrer Zelle und dem Einspeisen fremder Informationen in die eigene DNA schützen wollen.
Bildstrecke - AIDS-Impfstoff aus Algen
Die Geschichte in Bildern: Klicken Sie sich hier durch unsere Bildstrecke zum Thema!
Bildquelle: © nobeastsofierce/Fotolia.com
Eine weitere Schwierigkeit stellt die Identifizierung der Algen dar, welche eine Erbgutveränderung erfahren haben. Denn auch wenn Transgene relativ problemlos in das Genom des Zellkerns integriert werden können, gestaltet sich die Auswahl der transgenen Algen im Nachgang als mühselig. Gängige antibiotische Selektionsmarker funktionieren in der Grünalge nicht. Dadurch fällt es schwer, die Nadel im Heuhaufen zu finden, also die Algen, die das Fremdgen tragen und in ein Protein übersetzen.
Chlamydomonas wird konkurrenzfähig
Um die im Süßwasser vorkommende Grünalge Chlamydomonas reinhardtii mit anderen biotechnologischen Produktionsplattformen wettbewerbsfähig zu machen, arbeiten Wissenschaftler vom Max-Planck-Institut für Molekulare Pflanzenphysiologie in Potsdam-Golm daran, Algenstämme zu erzeugen, die Fremdgene effektiver in Proteine übersetzen.
Transgene an die Algenvorlieben angepasst
Die Forscher haben zunächst eine Geninformation optimiert, die dazu genutzt werden kann, ein für unser Immunsystem gut erkennbares Antigen des HI-Virus (p24) in Algen produzieren zu lassen. Auf diese Weise kann die Geninformation von den Algen „verstanden“ und in das entsprechende Protein übersetzt werden. Hierfür veränderten die Forscher die Sequenz des Gens derart, dass sie den typisch hohen GC-Gehalt des Algenerbguts aufwies. Denn Gene im Zellkerngenom von Chlamydomonas reinhardtii mit niedrigem GC-Gehalt werden nur schwach oder gar nicht abgelesen. Für die Ablesehäufigkeit eines Gens spielt außerdem die Codonauswahl für eine Aminosäure eine wichtige Rolle. Auch diesen Punkt optimierten die Forscher und passten die Codons des Transgens den natürlichen Algencodons an.
Um die Auswahl transgener Algen zu verbessern, passten die Forscher auch den GC-Gehalt und die Codonauswahl des geläufigen antibiotischen Resistenz- und Markergens Neomycin Phosphotransferase II (nptII) an die Vorlieben von Chlamydomonas reinhardtii an.
Effektiver Expressionsstamm gezüchtet
„Außerdem haben wir einen Algenstamm gezüchtet, der die fremden Gene besser ablesen kann“, erklärt Dr. Juliane Neupert, Wissenschaftlerin am Golmer Institut. Das fremde, optimierte Gen, das als potentieller Bestandteil für einen AIDS-Impfstoff gilt, wurde daraufhin in den neuen Algenstamm (UVM11) eingefügt- und bewährte sich in der Praxis.
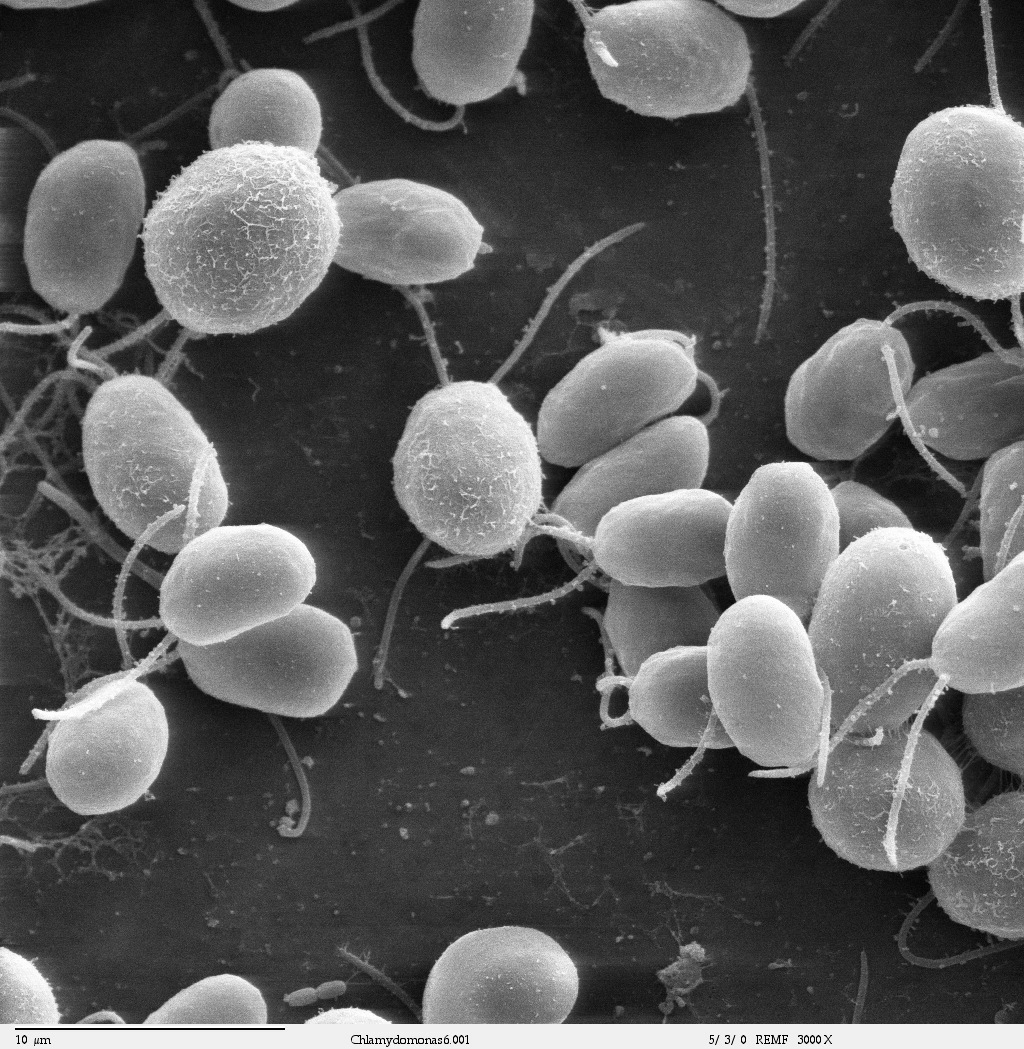
Die einzellige Grünalge Chlamydomonas reinhardtii (hier in elektronenmikroskopischer Aufnahme) eignet sich dank aktueller Forschungsarbeiten nun sehr gut zur Herstellung von Antigenen zur Impfstoffherstellung.
Bildquelle: © Dartmouth Electron Microscope Facility, Dartmouth College / Wikimedia.org/ CC0
HIV-Impfstoff dringend benötigt
Weltweit haben sich bisher geschätzte 78 Millionen Menschen mit dem HI-Virus infiziert - ein Virus, an dem bereits mehr als 39 Millionen Menschen gestorben sind. Da sich jährlich vor allem in Entwicklungsländern etwa 2 Millionen Menschen neu mit dem HI-Virus infizieren, arbeiten Wissenschaftler unter Hochdruck an einem Impfstoff. In der mehr als 30-jährigen HIV-Forschung konnten bereits Virusproteine identifiziert werden, die effizient von unserem Immunsystem erkannt werden und somit Bestandteil eines zukünftigen Impfstoffes sein könnten. Eines dieser Proteine ist das sogenannte p24-Protein.
„Wir konnten eine optimierte p24-Genvariante herstellen, die wir mit Hilfe gentechnischer Methoden in den verbesserten Chlamydomonas-Stamm eingebaut haben“, erklärt Rouhollah Barahimipour, Erstautor der Studie. „Die Alge war nun tatsächlich in der Lage, dieses verbesserte Gen abzulesen und das p24-Protein anzureichern“, bestätigt er.
Alge mit vielversprechender Zukunft
Die Golmer Forscher konnten die Hauptursachen für die bisherigen Probleme bei der Bildung fremder Proteine in Chlamydomonas aufklären und gleichzeitig eine neue Strategie zur effizienten Proteinproduktion in dieser Alge entwickeln. Ihre Arbeit zeigt, dass das System Alge eine vielversprechende Zukunft in der Biotechnologie hat. Sobald ein neuer Impfstoff gefunden ist, besteht nun die Möglichkeit, diesen in der Alge schnell und effizient zu produzieren.
Quelle: Barahimipour, R. et al. (2016): Efficient expression of nuclear transgenes in the green alga Chlamydomonas: synthesis of an HIV antigen and development of a new selectable marker. In: Plant Molecular Biology (8. Januar 2016), doi:10.1007/s11103-015-0425-8
Weiterlesen auf Pflanzenforschung.de:
- Biopharming - Pflanzenbasierte Arzneimittelproduktion
- Pflanzen für die Medizin - Algenextrakt gegen Krebs und Esskastanien gegen Keime (MRSA)
- Pflanzen als Pheromon-Fabriken - Pheromone aus Tabakpflanzen wirken effektiv gegen Gespinstmotten
Titelbild: Chlamydomonas reinhardtii - eine einzellige Grünalge: Test auf erfolgreiche Integration fremder Geninformation für die Herstellung eines potentiellen AIDS-Impfstoffs. (Bildquelle: © Rouhollah Barahimipour)
