Fast wie Lego
Rezeptoren und Hilfsmoleküle arbeiten gemeinsam an der Signalweiterleitung
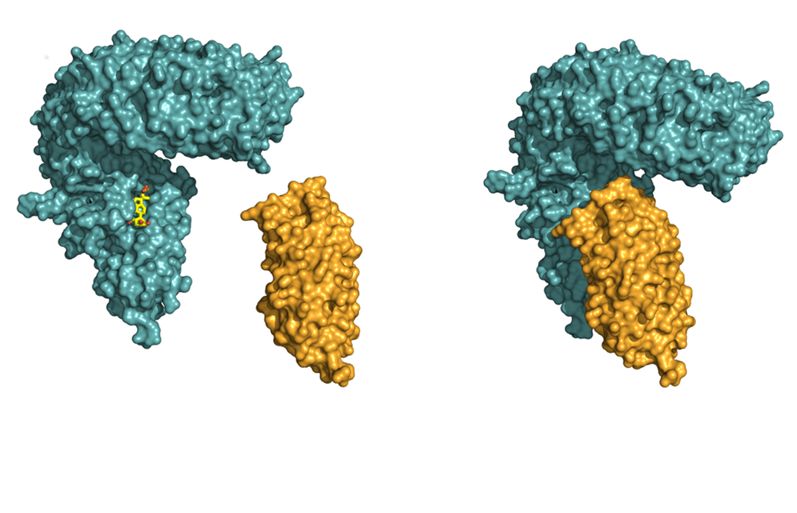
LRR-Domäne des Rezeptors BRI1 (blau), Hilfsrezeptors (orange). Im ersten Schritt bindet BRI1 das Steroidhormon (in gelb) in einer Tasche an seiner Oberfläche. (Quelle: © Julia Santiago)
LRR-Rezeptor-Kinasen sind eine überaus erfolgreiche Proteinfamilie der Pflanzen. Sie erkennen Pathogene, vermitteln die Zusammenarbeit mit Symbionten und sind an Wachstum und Entwicklung beteiligt. Auf Röntgen-Strukturaufnahmen wird jetzt erstmals sichtbar, dass die Rezeptoren bei der Signalweiterleitung nicht allein sind.
Wenn eine Zelle ein Haus wäre, dann wären Rezeptorproteine die neugierigen Nachbarn, die den ganzen Tag aus dem Fenster schauen und die Informationen von der Straße ins Innere der Wohnung tragen. Doch während wir auf Klatsch und Tratsch im Hausflur verzichten könnten, sind Rezeptorproteine für Zellen unabdingbar.
Rezeptoren bei Tieren sind bereits gut erforscht, doch über die Signalweiterleitung bei Pflanzen weiß man bisher nur wenig. Michael Hothorn und seine Mitarbeiter wollen das ändern. Seit fünf Jahren forscht Hothorn bereits an pflanzlichen Rezeptoren. Er vergleicht sie mit den Augen und Ohren der Zelle, die drei grundlegende Aufgaben haben: Sie müssen erstens ein Signal von außen wahrnehmen, zweitens das Signal ins Zellinnere weiterleiten und drittens eine Antwort auf das Signal auslösen.

Die Autoren der Veröffentlichung. Von links nach rechts: Julia Santiago (Postdoktorandin und Stipendiatin der Federation of European Biochemical Societies), Christine Henzler (technische Assistentin) und Michael Hothorn vom Friedrich Miescher Laboratorium der Max Planck Gesellschaft.
Bildquelle: © MPG
Das Signalmolekül selbst sorgt dafür, dass die Nachricht ins Zellinnere weitergeleitet wird
In ihren Untersuchungen konzentrierten sich die Forscher zuletzt besonders auf den pflanzlichen Rezeptor BRI1, der Wachstum und Entwicklung von Pflanzen steuert. Dieser Rezeptor arbeitet nicht gern allein. Damit er ein Signal ins Zellinnere weiterleiten kann, braucht er die Unterstützung des Proteins SERK1. Die Familie von SERK-Proteinen stand schon länger im Verdacht, Rezeptoren zu unterstützen, denn „soweit wir wissen, kann SERK selbst keine eigenen Liganden binden“, erklärt Hothorn.
Er und seine Arbeitsgruppe vom Friedrich-Miescher-Laboratorium der Max-Planck-Gesellschaft in Tübingen konnten jetzt zeigen, dass BRI1 und SERK1 nicht von alleine zusammenfinden, sondern erst das Signalmolekül selbst den Rezeptor und das Hilfsprotein zusammenbringt. Wie doppelseitiges Klebeband liegt das Steroidhormon Brassinolid zwischen BRI1 und SERK und ermöglicht damit die Signalweiterleitung ins Zellinnere.
Pflanzliche Steroidhormone bleiben lieber draußen
BRI1 gehört zur Gruppe der LRR-Rezeptor-Kinasen, die nur in Pflanzen vorkommen. Sie verdanken ihren Namen leucinreichen Sequenzen (engl. leucine-rich repeats) auf der Zellaußenseite. Allein in der Modellpflanze Arabidopsis thaliana sind mehrere hundert LRR-Rezeptor-Kinasen bekannt. „Das Proteinkonstrukt ist unglaublich erfolgreich, denn Pflanzen können damit die unterschiedlichsten Moleküle erkennen“, erklärt Hothorn.
Zum Beispiel Brassinosteroide, pflanzliche Wachstumshormone, die von der Struktur her den menschlichen Steroidhormonen wie Cortisol oder Testosteron ähneln. Bei Menschen und Tieren diffundieren die Steroidhormone direkt in den Zellkern und binden dort an Kernrezeptoren. Nicht so bei Pflanzen. „Wir sind uns immer noch nicht sicher, ob das pflanzliche Steroidhormon überhaupt durch die Zellmembran diffundieren kann“, so Hothorn.
Entweder hatten Pflanzen diese Kernrezeptoren nie oder sie hatten einen sehr guten Grund dafür, sie wieder loszuwerden
Dazu würde passen, dass Pflanzen keine Steroidrezeptoren im Zellkern besitzen. Entweder hatte der gemeinsame Vorfahre von Pflanzen und Tieren diese Klasse von Rezeptoren noch nicht oder die Pflanzen haben die Rezeptoren im Laufe der Entwicklung abgestoßen.
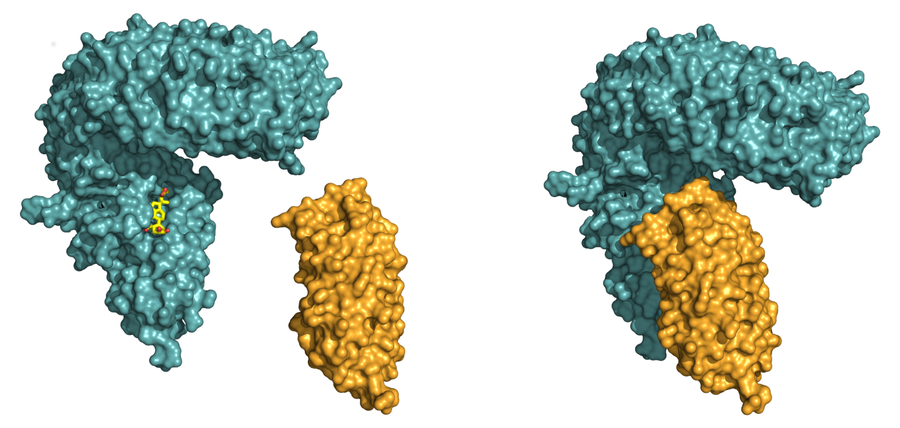
Aktivierung des pflanzlichen Brassinosteroid-Signalweges. (Links) Röntgenstrukturmodell der LRR-Domäne des Rezeptors BRI1 (in blau). Im ersten Schritt bindet BRI1 das Steroidhormon (in gelb) in einer Tasche an seiner Oberfläche. Danach kann dann die kleinere LRR-Domäne des Hilfsrezeptors (in orange) gebunden werden, das Hormon hält die beiden Eiweiße wie ein Klebstoff zusammen (Rechts).
Bildquelle: © Julia Santiago
Die Untersuchungen legen nahe, dass BRI1 mit mindestens drei unterschiedlichen Hilfsproteinen zusammenarbeiten kann und auch SERK1 mit mehreren Rezeptoren kompatibel ist. Wie in einem Lego-Baukasten lassen sich so Rezeptoren und Hilfsmoleküle immer wieder neu kombinieren. Hothorn glaubt nicht, dass dieses System zufällig entstanden ist. Wenn SERK1 gerade in einem Signalweg gebraucht wird, kann es nicht gleichzeitig in einem anderen mithelfen. „Die verschiedenen Signalwege beeinflussen sich auf diese Weise gegenseitig“, so Hothorn.
Ein besseres Verständnis von dem Zusammenspiel aus Rezeptoren und Signalmolekülen könnte einmal die Synthese von künstlichen Signalmolekülen erleichtern, mit deren Hilfe bestimmte Signalwege an- oder abgeschaltet werden können. Dadurch ließen sich komplexe Lebensprozesse gezielt verändern. Wachstums- oder Differenzierungsprozesse ließen sich besser steuern, Abwehrreaktionen verstärken oder abschwächen oder die Anpassung an Umweltbedingungen optimieren, so dass die Pflanzen nicht bei jeder Wolke am Himmel auf Reserve schalten, wodurch sich Ertragspotenziale erschließen ließen.
Quelle:
Santiago et al. (2013): Molecular Mechanism for Plant Steroid Receptor Activation by Somatic Embryogenesis Co-Receptor Kinases. In: Sciencexpress (Online-Veröffentlichung am 08. August 2013). doi: 10.1126/science.1242468.
Zum Weiterlesen auf Pflanzenforschung.de:
Phytohormone – Die Signalgeber des Pflanzenreichs
Titelbild: LRR-Domäne des Rezeptors BRI1 (blau), Hilfsrezeptors (orange). Im ersten Schritt bindet BRI1 das Steroidhormon (in gelb) in einer Tasche an seiner Oberfläche. (Quelle: © Julia Santiago)
