Leben retten mit Algen

Algen dienen als Produktionsplattform für Medikamente. (Quelle: © iStockphoto.com/Frank schoettke)
Fast die Hälfte aller Menschen auf der Erde ist von Malaria bedroht. Für die große Mehrheit dieser Menschen sind Medikamente unerschwinglich. Forschern gelang nun die kostengünstige Produktion eines vielversprechenden Malaria-Impfstoffs in Algen, der die Ausbreitung der verheerenden Krankheit verhindern könnte.
Malaria fordert jährlich weltweit etwa eine Million Todesopfer. In insgesamt 105 Ländern bedroht die Krankheit 3,3 Milliarden Menschen – etwa die Hälfte der Weltbevölkerung. In den Entwicklungsländern zählt Malaria zu den Haupttodesursachen, vor allem bei Kindern unter fünf Jahren. Die von Malaria betroffenen tropischen und subtropischen Gebiete gehören zu den ärmsten der Welt. Ein Impfstoff, der die Ausbreitung der Krankheit verhindern könnte, müsste nicht nur wirksam und sicher, sondern auch kostengünstig herzustellen sein.
Tropenmedizin trifft Biotechnologie
Stechmücken der Gattung Anopheles übertragen Malaria.
Bildquelle: © iStockphoto.com/Vladimír Vítek
Wissenschaftler, haben in Algen ein geeignetes Produktionssystem für einen möglichen Malaria-Impfstoff entdeckt und bereits erfolgreich erprobt. Dazu haben sich zwei Forschungsgruppen zu einer zunächst ungewöhnlichen Kollaboration zusammengeschlossen: Wissenschaftler aus dem Bereich der tropischen Medizin vereinten ihr Knowhow mit dem von Biotechnologen, die eigentlich Algen zur Biospritherstellung umfunktionieren. Das Resultat kann sich sehen lassen. Die Arbeitsgemeinschaft produzierte in Algen Proteine, die Labormäuse zur Antikörperproduktion gegen den Malariaerreger anregten. Ein derartig kostengünstig produzierter Impfstoff könnte die Übertragung von Malaria verhindern.
Algen: Effizient und günstig
Einen Malaria-Impfstoff herzustellen ist nicht ganz einfach. Die Proteine müssen den komplex aufgebauten, dreidimensionalen Proteinen, die die Malaria auslösenden Parasiten herstellen, ähneln. Nur dann bildet das menschliche Immunsystem nach einer Impfung passende Antikörper aus. Bakterien scheiden hierbei als Produktionsstätte aus, da sie derart komplexe Proteine nicht falten können. Menschliche Zellkulturen sind dazu zwar grundsätzlich in der Lage, verteuern die Herstellung aber erheblich gegenüber einer bakteriellen Produktion. „Mit den herkömmlichen Produktionsmethoden für Impfstoffe kann man nicht die Hälfte der Weltbevölkerung impfen. Das wäre unbezahlbar!“, erklärt Stephen Mayfield, Biologieprofessor an der University of California und Leiter des Forschungsprojektes. „Ein Malariaimpfstoff wird nur dann von Nutzen sein, wenn er zu einem Bruchteil der heutigen Produktionskosten für einen Impfstoff hergestellt werden kann. Algen verfügen über dieses Potential, denn man kann sie an jedem Platz auf der Welt in Becken oder sogar in Badewannen züchten“, so Mayfield.
Neben dem Kostenfaktor gibt es noch ein anderes Problem bei der Herstellung von Antikörpern gegen Malaria. „Der Malaria auslösende Parasit produziert zwar komplexe Proteine, hängt aber aus irgendwelchen Gründen keine Zuckerreste an“, erklärt Mayfield.
Menschliche Zellkulturen würden die fertigen Proteine aber mit einem Zuckerrest versehen, was sie als Impfstoffe unbrauchbar machte. Bei sog. glykosilierten Proteinen bildet der Körper nämlich meist Antikörper gegen den Zuckerrest, nicht gegen das eigentliche Protein.
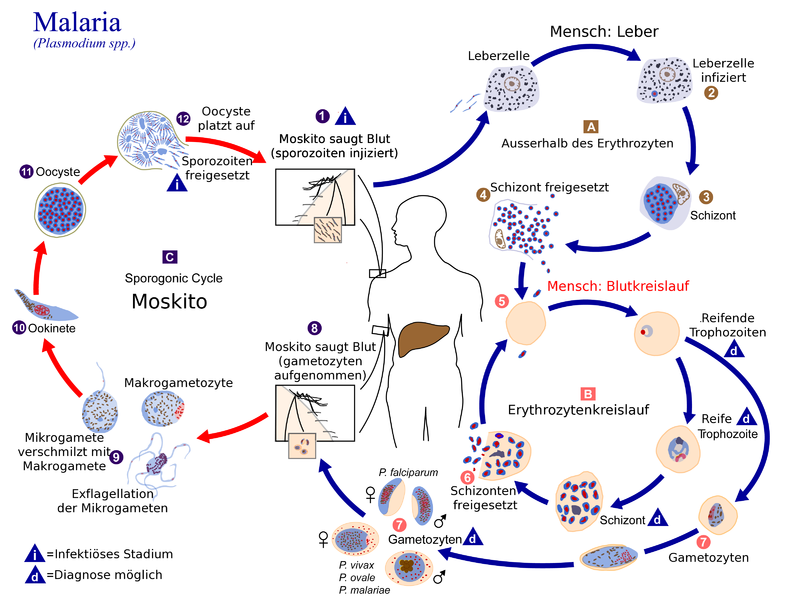
Der Lebenszyklus der Plasmodien - Der Mensch dient dabei lediglich als Zwischenwirt.
Bildquelle: © Chb / wikimedia.org; gemeinfrei
Die essbare Grünalge Chlamydomonas reinhardtii scheint die Lösung derartiger Produktionsprobleme zu sein. Wie das Bakterium E. coli und die Fruchtfliege Drosophila dient sie in zahlreichen Laboratorien als genetischer Modellorganismus. Dass diese Alge grundsätzlich in der Lage ist, komplexe menschliche Proteine wie Wachstumshormone oder monoklonale Antikörper herzustellen, zeigten die Wissenschaftler bereits vor zwei Jahren. Und auch die Herstellung der Oberflächenproteine PFs25 und Pfs28 des Malaria auslösenden Parasiten Plasmodium falciparum meisterte die Alge erfolgreich. Antikörper, die diese Oberflächenproteine erkennen, durchbrechen den sexuellen Vermehrungszyklus des einzelligen Parasiten im Darm der Stechmücke und verhindern so die Ausbreitung der Krankheit.
Vielversprechender Impfstoff
In Zusammenarbeit mit einem führenden Experten für Tropenkrankheiten, Joseph Vinetz, konnten die Wissenschaftler die Wirksamkeit ihrer in Algen produzierten rekombinanten Proteine zeigen. Wenn sie diese Proteine den Labormäusen spritzten, produzierten die Tiere Antikörper, die die Oberflächenproteine Pfs25 und Pfs28 des Parasiten Plasmodium falciparum erkannten. Diese Antikörper banden erfolgreich an die Oberfläche von in vitro kultivierten Parasiten im sexuellen Vermehrungsstadium und könnten so die Malariaübertragung durch Stechmücken verhindern.
„Ob die von uns in Algen hergestellten Proteine perfekt sind, weiß ich natürlich nicht. Aber wir haben brauchbare Impfstoffkandidaten produziert und wir haben theoretisch die Möglichkeit, damit unzählig viele Menschen zu impfen“, resümiert Mayfield. „Mit keinem anderen Produktionssystem würde es sich lohnen, auch nur darüber nachzudenken!“
Ob der vielversprechende Impfstoff tatsächlich die Ausbreitung von Malaria verhindern kann, müssen die Wissenschaftler allerdings erst noch testen. Wenn das gelingt, könnten die Proteine vielleicht sogar derart verändert werden, dass sie auch beim Verzehr der Algen wirksam wären und nicht injiziert werden müssten.
Quelle:
Gregory J.A. et al.(2012): Algae-produced pfs25 elicits antibodies that inhibit malaria transmission. In: PLoS One. 2012;7(5):e37179, 16. Mai 2012, doi:10.1371/journal.pone.0037179.
Weiterlesen auf Pflanzenforschung.de:
